治験コーディネーター(CRC)とは
CRC(Crinical Research Coordinator)の定義
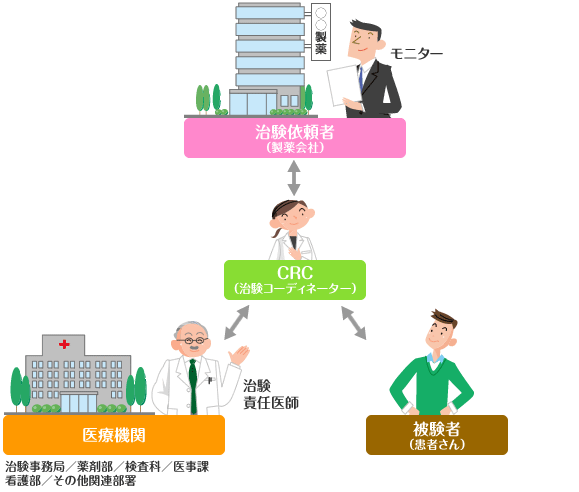
厚生省令GCP第2条において、「治験実施医療機関において、治験責任医師または治験分担医師の下で治験に係る業務に協力する薬剤師、看護師、その他の医療関係者をいう」と規定されています。 CRCは看護師、薬剤師、その他の医療関係者があたる事が多く、院長の承認を受け、治験依頼者(モニター)や医療機関内のスタッフ、治験責任医師、治験分担医師、治験薬管理者、検査部門担当者、医事課、病歴室スタッフ他ならびに、被験者との間を調整(コーディネート)する役割を担っています。院内にCRCがいない場合、CRCは専門の会社から派遣される事が多く、病院とCRCの所属会社間で契約を締結して院内で作業を行います。
CRCの業務内容
治験説明会出席
| 業務を開始するにあたり、治験依頼者の担当者(モニター)より治験実施計画書の内容について説明を受けます。
|
治験開始の準備
| 治験責任医師とCRC業務に関する事前協議、院内各部署の情報収集
治験資材(外注検査キット・症例ファイル等)の搬入・管理、治験薬搬入時の立会い CRC資料作成(業務手順書の作成・被験者ファイルの準備) |
スタートアップ・ミーティング
| 医療機関で治験を開始するにあたり、院内関係者(医師、検査科等)およびCRCが一堂に会し、お互いの役割分担、治験スケジュールなどの最終確認を行います。
|
被験者候補選択
適格性確認作業 | 対象疾患、選択基準、除外基準による患者の選択リストの作成、医師への報告・打ち合わせ
|
同意説明補助
| ---
|
被験者の治験登録補助
| ---
|
被験者対応
| 医師の指示のもとに被験者の生活指導・教育、被験者の相談窓口
|
医師への支援
| ---
|
プロトコールに沿った来院日・検査スケジュールの管理
| 医師への情報・資料の提供、当日の検査、観察項目、治験依頼者からの資料の提供
|
検査データの収集および整理
| データの異常値発見の場合医師への報告、データの整合性等のチェック
|
症例報告書(CRF)の作成支援
| 原資料に基づき医学的判断を伴わない部分の支援
|
有害事象への対応
| 治験責任医師への報告、重篤な副作用情報の報告資料の作成
|
モニタリング、SDV、監査への対応
| ---
|
資料等の保管補助
| 原資料やGCPで定められている保存すべき書類(必須文書)の保管、整理の支援
|
その他
| 被験者の治験参加に伴う負担軽減費や保険外併用療養費関係への支援
|
CRCに求められるもの
CRCが医療機関内で仕事を行う時、求められる3つの要素は・・・
①知識
臨床試験の知識、疾患の知識、GCPの知識、医薬品の知識
②態度
医療人、社会人としての態度
③技術
患者さんへのインフォームドコンセント、スケジュール管理や被験者のケア
薬剤部・検査部・治験担当医師など治験に関わるチーム内の調整・書類の整理
症例報告書の作成(データ管理)・コミュニケーション技術
- コミュニケーション能力が高いことが、CRCには求められるのです。
自分中心に考えるのではなく、相手の立場・状況に配慮した言動に気をつけましょう。
伝えるべき内容をわかりやすく、きちんと伝えられるように、相手に説明する時は工夫しましょう。 - 明るく笑顔で挨拶ができ、誠実な応対をすることが大切です。
- 医療機関で働く者として、身だしなみは大切です。派手な服装やメイクは避けましょう。
私たちCRCは、「縁の下の力持ち」となり、良いお薬を待ち望む患者さま達が、一日でも早く薬が使えるように、多忙な医療現場で治験業務の円滑化をはかり、サポートしています。
人と接することが好きで、何事にも熱心で向上心のある方、私たちと一緒に患者さん、医療機関の方、治験依頼者の方から「ありがとう」といわれるCRCを目指しませんか?
「CRCのための治験業務マニュアル 第2版」をじほうより出版しています。
人と接することが好きで、何事にも熱心で向上心のある方、私たちと一緒に患者さん、医療機関の方、治験依頼者の方から「ありがとう」といわれるCRCを目指しませんか?
「CRCのための治験業務マニュアル 第2版」をじほうより出版しています。

